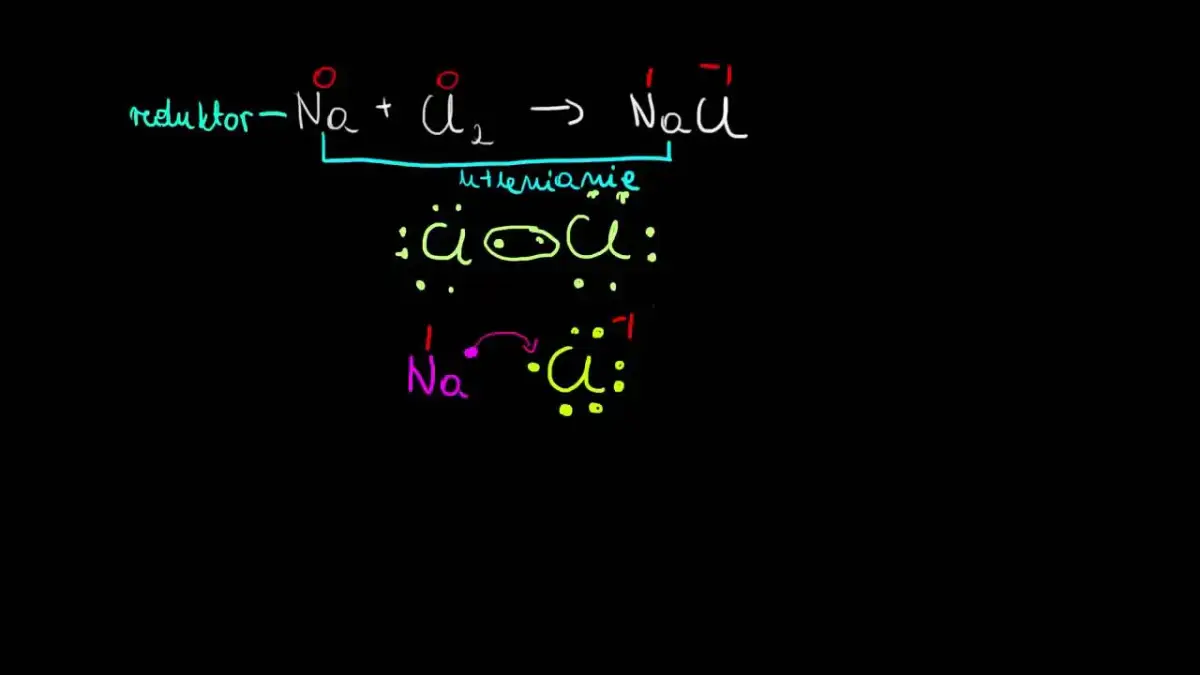Reduktor w chemii to kluczowy element w reakcjach redoks, który odgrywa istotną rolę w wielu procesach chemicznych. Jest to pierwiastek lub związek chemiczny, który działa jako donor elektronów, co prowadzi do zwiększenia jego stopnia utlenienia. W tym artykule przyjrzymy się bliżej, czym dokładnie jest reduktor, jakie ma znaczenie oraz jakie przykłady można znaleźć w świecie chemii.
W chemii reduktory są niezwykle ważne, ponieważ wpływają na zachowanie się innych substancji w reakcjach. Przykłady silnych reduktorów obejmują metale alkaliczne, takie jak sód, magnez i cynk, a także wodór. Rozumienie ich funkcji i zastosowań pozwala lepiej zrozumieć procesy chemiczne zachodzące w naszym otoczeniu.
Kluczowe informacje:- Reduktor to donor elektronów w reakcjach redoks.
- Podczas reakcji reduktory zwiększają swój stopień utlenienia.
- Silne reduktory to m.in. metale alkaliczne i wodór.
- Węgiel i jego tlenek mogą również działać jako reduktory w odpowiednich warunkach.
- Reduktory mają kluczowe znaczenie w wielu procesach chemicznych i przemysłowych.
Co to jest reduktor w chemii i jego podstawowe znaczenie
Reduktor w chemii to pierwiastek lub związek chemiczny, który w reakcjach redoks działa jako donor elektronów. W procesie tym reduktory zwiększają swój stopień utlenienia, co oznacza, że oddają elektrony innym substancjom. W ten sposób powodują zmniejszenie stopnia utlenienia w pozostałych produktach reakcji, co jest kluczowe dla wielu procesów chemicznych.
Bez reduktorów nie mogłyby zachodzić ważne reakcje chemiczne, takie jak te, które prowadzą do syntez chemicznych czy procesów energetycznych. Przykłady silnych reduktorów obejmują metale alkaliczne, takie jak sód, magnez i cynk, a także wodór oraz wodorki metali alkalicznych. W zależności od warunków, także węgiel i jego tlenek mogą pełnić rolę reduktorów.Definicja reduktora i jego rola w reakcjach redoks
Reduktor to substancja, która oddaje elektrony w trakcie reakcji chemicznych, co czyni go kluczowym elementem w reakcjach redoks. W takich reakcjach dochodzi do wymiany elektronów między dwoma reagentami, gdzie jeden reagent działa jako reduktor, a drugi jako utleniacz. W wyniku tego procesu reduktor zmienia swój stopień utlenienia, co jest istotne dla zrozumienia mechanizmów reakcji chemicznych.
W praktyce oznacza to, że reduktor wpływa na przemiany chemiczne i ich efektywność. Na przykład, w reakcjach organicznych, reduktory są wykorzystywane do przekształcania związków w bardziej złożone lub prostsze formy. Ich rola jest nieoceniona w przemyśle chemicznym, gdzie redukcja jest kluczowym krokiem w produkcji wielu substancji.
Jakie są różnice między reduktorami a utleniaczami?
Reduktory i utleniacze pełnią przeciwstawne role w reakcjach redoks. Reduktory oddają elektrony, natomiast utleniacz je przyjmuje. To sprawia, że w każdej reakcji chemicznej zachodzi równocześnie proces redukcji i utlenienia. Na przykład, w reakcji między wodorem a tlenem, wodór działa jako reduktor, a tlen jako utleniacz. Zrozumienie tych różnic jest kluczowe dla analizy i przewidywania wyników reakcji chemicznych.
Przykłady silnych i słabych reduktorów w chemii
W chemii istnieje wiele rodzajów reduktorów, które różnią się swoją siłą oraz zastosowaniem. Silne reduktory mają zdolność do łatwego oddawania elektronów, co czyni je niezwykle efektywnymi w reakcjach redoks. Z drugiej strony, słabe reduktory oddają elektrony trudniej i są stosowane w bardziej specyficznych warunkach. Zrozumienie tych różnic jest kluczowe dla zastosowania reduktorów w praktyce chemicznej.
Wśród silnych reduktorów można wymienić metale alkaliczne, takie jak sód, magnez i cynk. Wodór i jego związki, takie jak wodorek sodu czy wodorek litowo-glinowy, również wykazują silne właściwości redukcyjne. Ich zastosowanie jest szerokie, od przemysłu chemicznego po procesy biologiczne, gdzie odgrywają kluczową rolę w redukcji chemicznej.
Najczęściej stosowane silne reduktory i ich właściwości
Silne reduktory, takie jak sód, mają wyjątkową zdolność do oddawania elektronów. Na przykład, sód w reakcji z wodą tworzy wodorotlenek sodu i uwalnia wodór, co jest doskonałym przykładem jego właściwości redukcyjnych. Magnez jest kolejnym silnym reduktorem, który często stosuje się w reakcjach z tlenkami metali, przekształcając je w czyste metale. Cynk z kolei jest wykorzystywany w procesach galwanizacji, gdzie działa jako reduktor, chroniąc inne metale przed korozją.
Oto tabela przedstawiająca niektóre z najczęściej stosowanych silnych reduktorów oraz ich właściwości:
| Reduktor | Właściwości | Zastosowanie |
| Sód | Silny reduktor, reaguje z wodą | Produkcja wodorotlenków |
| Magnez | Reaguje z tlenkami metali | Produkcja metali |
| Cynk | Chroni przed korozją | Galwanizacja |
Słabe reduktory: kiedy i jak są wykorzystywane?
Słabe reduktory oddają elektrony w mniej efektywny sposób, co czyni je przydatnymi w specyficznych reakcjach chemicznych. Przykłady słabych reduktorów to niektóre metale przejściowe, takie jak żelazo i miedź, które w odpowiednich warunkach mogą działać jako reduktory. Ich zastosowanie obejmuje procesy, gdzie kontrola nad reakcją jest kluczowa, na przykład w syntezach organicznych czy w reakcjach katalitycznych.
Znaczenie reduktorów w procesach chemicznych i przemysłowych

Reduktory odgrywają kluczową rolę w procesach chemicznych oraz przemysłowych, wpływając na efektywność wielu reakcji. Dzięki swojej zdolności do oddawania elektronów, są niezbędne w reakcjach redoks, które są fundamentem wielu procesów, takich jak synteza chemiczna, produkcja energii oraz oczyszczanie substancji. Ich obecność umożliwia przekształcanie surowców w bardziej wartościowe produkty, co jest istotne w różnych dziedzinach przemysłu.
W przemyśle chemicznym wykorzystanie reduktorów jest niezbędne do przeprowadzania reakcji, które wymagają redukcji. Na przykład, w produkcji metali z ich tlenków, reduktory są kluczowe dla przekształcenia surowców w czyste metale. Ponadto, w branży farmaceutycznej, reduktory są stosowane do syntez organicznych, co pozwala na tworzenie skomplikowanych cząsteczek leków.
Praktyczne zastosowania reduktorów w przemyśle chemicznym
Przykłady zastosowań reduktorów w przemyśle chemicznym są liczne i różnorodne. W procesie produkcji stali, węgiel jest używany jako reduktor, który przekształca tlenki żelaza w czyste żelazo. Dzięki temu procesowi, możliwe jest uzyskanie wysokiej jakości stali, która jest podstawowym materiałem budowlanym. Inny przykład to zastosowanie wodoru w procesie hydrorafinacji, gdzie działa jako reduktor, usuwając zanieczyszczenia z olejów ropopochodnych.
Oto tabela przedstawiająca kilka zastosowań reduktorów w przemyśle chemicznym:
| Reduktor | Zastosowanie | Proces |
| Węgiel | Produkcja stali | Redukcja tlenków żelaza |
| Wodór | Hydrorafinacja | Usuwanie zanieczyszczeń z olejów |
| Magnez | Produkcja metali | Redukcja tlenków metali |
Jak reduktory wpływają na reakcje chemiczne i ich efektywność?
Reduktory mają istotny wpływ na efektywność reakcji chemicznych. Dzięki swojej zdolności do oddawania elektronów, przyspieszają procesy chemiczne, co prowadzi do szybszego uzyskania pożądanych produktów. Na przykład, w reakcjach organicznych, obecność silnych reduktorów może znacznie zwiększyć wydajność syntez, co jest kluczowe dla przemysłu farmaceutycznego.
Warto również zauważyć, że odpowiedni dobór reduktora ma znaczenie dla jakości końcowego produktu. Zastosowanie niewłaściwego reduktora może prowadzić do niepożądanych reakcji ubocznych, co z kolei wpływa na efektywność całego procesu chemicznego. Dlatego tak ważne jest, aby chemicy dokładnie analizowali właściwości chemiczne reduktorów przed ich zastosowaniem w praktyce.Kluczowa rola reduktorów w efektywności procesów chemicznych
Reduktory są niezbędne w procesach chemicznych i przemysłowych, gdzie ich zdolność do oddawania elektronów wpływa na efektywność wielu reakcji. Przykłady zastosowań, takie jak wykorzystanie węgla w produkcji stali czy wodoru w hydrorafinacji, pokazują, jak kluczowe jest ich zastosowanie w przemyśle. Właściwy dobór reduktora ma ogromne znaczenie dla jakości końcowego produktu, co podkreśla potrzebę dokładnej analizy właściwości chemicznych tych substancji.
Przyspieszanie reakcji chemicznych przez reduktory, jak w przypadku magnezu w redukcji tlenków metali, pokazuje ich wpływ na wydajność syntez. Zastosowanie silnych reduktorów może znacząco zwiększyć efektywność procesów, co jest kluczowe w przemyśle farmaceutycznym. Dlatego tak istotne jest, aby chemicy starannie wybierali reduktory, aby zminimalizować ryzyko reakcji ubocznych i maksymalizować efektywność reakcji chemicznych.